- CITY GUIDE
- PODCAST
-
 17°
17°
Η μακρά ιστορία των εμβολίων mRNA
Εκατοντάδες επιστήμονες είχαν εργαστεί σε εμβόλια mRNA επί δεκαετίες προτού η πανδημία του κορωνοϊού φέρει σημαντικές ανακαλύψεις

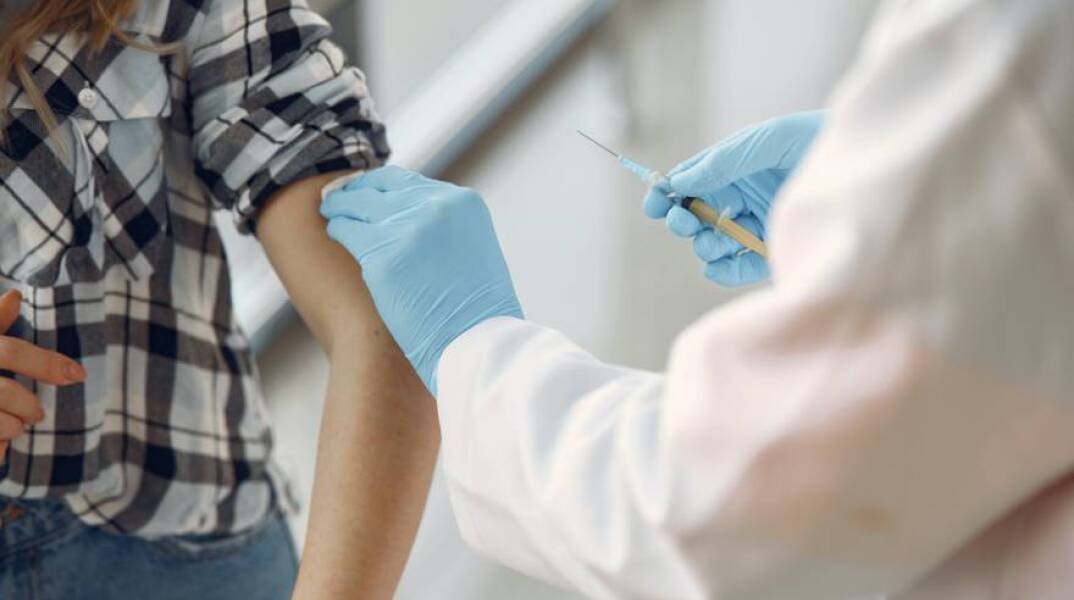
Εμβόλια mRNA: Πώς δημιουργήθηκαν, ποια ήταν συνεισφορά του Robert Malone και πώς φτάσαμε στα εμβλόλια κατά της Covid-19.
Στο τέλος του 1987, ο Robert Malone πραγματοποίησε ένα πείραμα που θεωρείται ορόσημο. Ανέμειξε σκέλη αγγελιοφόρου RNA με σταγονίδια λίπους, για να δημιουργήσει ένα είδος μοριακού στιφάδου. Ανθρώπινα κύτταρα λουσμένα σε αυτό το γενετικό υλικό απορρόφησαν το mRNA και άρχισαν να παράγουν πρωτεΐνες. Συνειδητοποιώντας ότι αυτή η ανακάλυψη θα μπορούσε να έχει μεγάλο αντίκτυπο στην ιατρική, ο Malone, μεταπτυχιακός φοιτητής στο Ινστιτούτο Βιολογικών Μελετών Salk στη Λα Τζόλα της Καλιφόρνιας, υπέβαλε ένα επιστημονικό paper όπου έγραφε ότι αν τα κύτταρα μπορούσαν να δημιουργήσουν πρωτεΐνες από το mRNA είναι πιθανό να το RNA να χρησιμοποιηθεί ως φάρμακο. Αργότερα, το 1988, ο Μalone έκανε πειράματα που έδειξαν ότι έμβρυα βατράχου απορροφούσαν τέτοιο mRNA. Ήταν η πρώτη φορά που κάποιος χρησιμοποιούσε λιπαρά σταγονίδια για να διευκολύνει τη μετάβαση του mRNA σε ζωντανό οργανισμό.

Αυτά τα πειράματα ήταν το σκαλοπάτι για δύο από τα πιο σημαντικά και κερδοφόρα εμβόλια στην ιστορία: τα εμβόλια COVID-19 με βάση το mRNA που δόθηκαν σε εκατοντάδες εκατομμύρια ανθρώπους σε όλο τον κόσμο. Οι παγκόσμιες πωλήσεις τους αναμένεται να ξεπεράσουν τα 50 δισεκατομμύρια δολάρια μέσα το 2021.
Αλλά ο δρόμος προς την επιτυχία είχε πολλά σκαβανεμπάσματα. Για πολλά χρόνια μετά τον Μalone, τα πειράματα, τα οποία είχαν βασιστεί στην εργασία άλλων ερευνητών, το mRNA θεωρήθηκε υπερβολικά ασταθές και ακριβό για να χρησιμοποιηθεί ως φάρμακο ή εμβόλιο. Δεκάδες ακαδημαϊκά εργαστήρια και εταιρείες εργάζονταν πάνω σ’ αυτή την ιδέα για να βρουν τη σωστή φόρμουλα λιπαρών και νουκλεϊκών οξέων: τα δομικά στοιχεία των εμβολίων mRNA.
Σήμερα τα ενέσιμα εμβόλια mRNA είναι αποτέλεσμα καινοτομιών που έγιναν από το τέλος της δεκαετίας του 1980 -όπως το χημικά τροποποιημένο RNA και οι διαφορετικοί τύποι φυσαλίδων λίπους για τη μεταφορά του στα κύτταρα. Αλλά ο Μalone, που αυτοαποκαλείται «εφευρέτης των εμβολίων mRNA», πιστεύει ότι το έργο του δεν έχει αναγνωριστεί επαρκώς. Κι εφόσον η πρόσφατη πανδημία αντιμετωπίστηκε με εμβόλια mRNA, είναι φυσικό να γίνεται λόγος για το Νόμπελ ιατρικής και βιολογίας σ’ αυτόν τον τομέα. Όμως, το θέμα είναι ότι η πορεία προς τα εμβόλια mRNA βασίστηκε στο έργο εκατοντάδων ερευνητών για περισσότερα από τριάντα χρόνια.
Έτσι συμβαίνει σχεδόν πάντοτε με τις μεγάλες ανακαλύψεις: οι άνθρωποι βασίζονται σε έργο άλλων και περπατούν σε ώμους γιγάντων: συχνά κυλούν δεκαετίες γεμάτες αδιέξοδα, αλλά και γενναιοδωρία, και περιέργεια και επιμονή μπροστά στον σκεπτικισμό, στην ηττοπάθεια και στην αμφιβολία. Όπως λέει ο Paul Krieg, εξελικτικός βιολόγος στο Πανεπιστήμιο της Αριζόνα στην Τουσόν, «ποτέ δεν ξέρεις τι θα αποβεί χρήσιμο για την ιατρική».

Όσο για τις απαρχές του mRNA, ήδη από το 1978, οι επιστήμονες είχαν χρησιμοποιήσει δομές λιπαρών μεμβρανών που ονομάζονταν λιποσώματα για να μεταφέρουν mRNA σε κύτταρα ποντικού και ανθρώπου για να προκαλέσουν την ανάπτυξη πρωτεΐνης. Με τη σειρά τους, αυτά τα πειράματα βασίστηκαν σε χρόνια εργασίας με λιποσώματα και mRNA από τη δεκαετία του 1960. Τότε, ωστόσο, λίγοι ερευνητές σκέφτονταν το mRNA ως ιατρικό προϊόν: δεν υπήρχε ακόμα τρόπος να παραχθεί γενετικό υλικό σε εργαστήριο. Το 1984 όμως, όταν ο Krieg και άλλα μέλη μιας ομάδας με επικεφαλής τον εξελικτικό βιολόγο Douglas Melton και τους μοριακούς βιολόγους Tom Maniatis και Michael Green στο Πανεπιστήμιο του Χάρβαρντ, χρησιμοποίησαν ένα ένζυμο σύνθεσης RNA (προερχόμενο από ιό) και άλλα εργαλεία για την παραγωγή βιολογικά ενεργού mRNA στο εργαστήριο: μια μέθοδος που, στον πυρήνα της, παραμένει σε χρήση μέχρι σήμερα. Αλλά, τότε, τόσο ο Melton όσο και ο Krieg λένε ότι είδαν το συνθετικό mRNA κυρίως ως ερευνητικό εργαλείο για τη μελέτη της γονιδιακής λειτουργίας και δραστηριότητας. Το 1987, αφού ο Melton διαπίστωσε ότι το mRNA θα μπορούσε να χρησιμοποιηθεί για την ενεργοποίηση και για την πρόληψη της παραγωγής πρωτεϊνών, πήρε μέρος στη δημιουργία μιας εταιρείας που ονομάζεται Oligogen (αργότερα μετονομάστηκε σε Gilead Sciences) στο Foster City της Καλιφόρνιας) για να διερευνήσει τρόπους χρήσης συνθετικού RNA στη θεραπεία ασθενειών. Δημιουργήθηκαν πολλές τέτοιες εταιρείες και επιστημονικές ομάδες οι οποίες εργάζονταν εντατικά παραμερίζοντας τον Malone ο οποίος δεν πήρε ποτέ το διδακτορικό του: τσακώθηκε με τον προϊστάμενό του, τον Jonas Salk, ερευνητή στην Inder Verma και, το 1989, εγκατέλειψε τις μεταπτυχιακές σπουδές και βρήκε δουλειά στην εταιρεία Vical στο Σαν Ντιέγκο. Ακολούθησαν πολλοί καβγάδες: η Vical (που συνεργαζόταν με το Πανεπιστήμιο του Ουισκόνσιν) και ο Jonaw Salk από την πλευρά του υπέβαλαν αίτηση για την πατέντα του mRNA τον Μάρτιο του 1989, ενώ ο Malone έφυγε από τη Vical τον Αύγουστο του 1989, επικαλούμενος διαφωνίες με τον συνεργάτη του P.L. Felgner σχετικά με την «επιστημονική κρίση» και την «πίστωση για τη συνεισφορά στην επιστήμη»: το 1996, υπέβαλε ανεπιτυχώς αίτηση σε κρατική ερευνητική υπηρεσία της Καλιφόρνιας προκειμένου να αναπτύξει εμβόλιο mRNA για την καταπολέμηση των εποχικών λοιμώξεων από κορωνοϊό. Αλλά καθώς κανείς δεν φαινόταν να του πιστώνει την ανακάλυψη άρχισε να καταφέρεται εναντίον των εμβολίων mRNA που προσπαθούσαν να δημιουργήσουν οι ανταγωνιστές του.

Το 1991, η Vical άρχισε να συνεργάζεται με την εταιρεία Merck, έναν από τους μεγαλύτερους κατασκευαστές εμβολίων. Οι επιστήμονες της Merck αξιολόγησαν την τεχνολογία mRNA σε ποντίκια με στόχο τη δημιουργία εμβολίου γρίπης, αλλά στη συνέχεια εγκατέλειψαν αυτήν την προσέγγιση λόγω του πολύ μεγάλου κόστους. Στο μεταξύ μια μικρή εταιρεία βιοτεχνολογίας στο Στρασβούργο, με επικεφαλής τον Pierre Meulien, έδειξε ότι το mRNA σε λιπόσωμα θα μπορούσε να προκαλέσει αντιιική ανοσοαπόκριση σε ποντίκια. Σχεδόν παραλλήλως, και ξεχωριστά, οι επιστήμονες στο Scripps Research Institute στη Λα Τζόλα χρησιμοποίησαν το mRNA στη θεραπεία μεταβολικής διαταραχής σε ποντίκια. Ο Pierre Meulien στο Στρασβούργο και η ομάδα της Merck, επικεντρώθηκαν σε εμβόλια DNA: αν και δεν προέκυψε εμβόλιο DNA, η τεχνολογία DNA ωφέλησε την έρευνα του RNA σε όλο τον κόσμο: ο Peter Liljeström, ιολόγος στο Ινστιτούτο Karolinska στη Στοκχόλμη, είναι από εκείνους που ασχολούνται με τα εμβόλια RNA από το 1991 -αλλά, υπήρχαν πολλοί ιολόγοι και βιολόγοι, όπως παραδέχεται σήμερα ο ερευνητής Matt Winkler, από το Όστιν του Τέξας, που δεν πίστευαν καθόλου στην προοπτική του ενέσιμου εμβολίου με RNA. Η ιδέα του εμβολίου mRNA συνάντησε πιο ευνοϊκή υποδοχή στους κύκλους της ογκολογίας, ως θεραπευτικός παράγοντας, όχι για την πρόληψη ασθενειών. Ξεκινώντας με το έργο του γονιδιακού θεραπευτή David Curiel, αρκετοί ακαδημαϊκοί επιστήμονες και νεοσύστατες εταιρείες διερεύνησαν αν το mRNA θα μπορούσε να χρησιμοποιηθεί για την καταπολέμηση του καρκίνου. Αν το mRNA κωδικοποιούσε πρωτεΐνες που εκφράζουν καρκινικά κύτταρα, μήπως μπορούσε η έγχυσή του στο σώμα να εκπαιδεύσει το ανοσοποιητικό σύστημα ώστε να επιτεθεί σε αυτά τα κύτταρα; Ακολούθησε πλήθος τέτοιων ερευνών σε όλον τον κόσμο· και παρότι η έρευνα προχώρησε δείχνοντας τα πλεονεκτήματα του τροποποιημένου mRNA, έπρεπε να περιμένουμε μέχρι τα πρώτα χρόνια του 21ου αιώνα όταν μια ομάδα με επικεφαλής τον Derrick Rossi, τότε βιολόγο βλαστοκυττάρων στο παιδιατρικό νοσοκομείο της Βοστόνης έπεισε τον επιστημονικό κόσμο: τροποποιημένο mRNA μπορούσε να κινητοποιήσει το ανοσοποιητικό σύστημα εναντίον των παθογόνων. Ακολούθησε πόλεμος εισηγήσεων και αιτήσεων για ευρεσιτεχνία: πολλές εταιρείες διεκδικούσαν την εφεύρεση -η Moderna, η UPenn, η BioNTech, η RNARx- ενώ παραλλήλως γίνονταν συγχωνεύσεις φαρμακευτικών εταιρειών και εργαστηρίων. Στον ανταγωνισμό συμμετείχε ο γαλλικός κολοσσός Sanofi, η Strand Therapeutics -μια επιχείρηση συνθετικής βιολογίας με έδρα το Κέιμπριτζ που εργάζεται σε θεραπείες με βάση το mRNA- και η κινεζική Abogen.
Tην τεχνολογία του mRNA βοήθησε η τεχνολογία των λιπιδικών νανοσωματιδίων, ή LNP, τα οποία προστατεύουν το mRNA και το μεταφέρουν στα κύτταρα. Αυτή η τεχνολογία προέρχεται από το εργαστήριο του Pieter Cullis, βιοχημικού στο Πανεπιστήμιο του Βανκούβερ. Τα νανοσωματίδια περιέχουν ένα μείγμα τεσσάρων λιπαρών μορίων: τρία συμβάλλουν στη δομή και τη σταθερότητα, ενώ το τέταρτο, που ονομάζεται ιονίζον λιπίδιο, είναι το κλειδί για την επιτυχία της LNP. Το κοκτέιλ των τεσσάρων λιπιδίων επιτρέπει στο προϊόν να αποθηκευτεί για μεγαλύτερο χρονικό διάστημα στο ράφι του φαρμακείου και να διατηρήσει τη σταθερότητά του μέσα στο σώμα, λέει ο Ian MacLachlan, πρώην στέλεχος σε πολλές επιχειρήσεις που συνδέονται με την Cullis. Στα μέσα της δεκαετίας του 2000, επινοήθηκε ένας καινούργιος τρόπος ανάμειξης και κατασκευής των νανοσωματιδίων με τη χρήση του λεγόμενου "T-connector" που συνδυάζει λίπη (διαλυμένα σε αλκοόλη) με νουκλεϊκά οξέα (διαλυμένα σε όξινο ρυθμιστικό διάλυμα). Αποδείχθηκε ότι αυτό ήταν μια πιο αξιόπιστη τεχνική από άλλους τρόπους παρασκευής φαρμάκων με βάση το mRNA.

Από τα τέλη της δεκαετίας του 2000, αρκετές μεγάλες φαρμακευτικές εταιρείες διέθεταν τμήμα έρευνας του mRNA. Το 2008, για παράδειγμα, τόσο η Novartis όσο και η Shire ίδρυσαν ερευνητικές μονάδες mRNA. Μέχρι το 2015 η Moderna είχε εξασφαλίσει χρηματοδότηση πάνω από 1 δισεκατομμύριο δολάρια με την υπόσχεση να αξιοποιήσει το mRNA ως ενεργοποιητικό στοιχείο του ανοσοποιητικού συστήματος: δηλαδή το mRNA θα «διόρθωνε» ασθένειες που προκαλούνται από ελλείψεις ή ελαττωματικές πρωτεΐνες. Αυτό το σχέδιο απέτυχε. Τότε η Moderna, με επικεφαλής τον Stéphane Bancel, επέλεξε να δώσει προτεραιότητα σε έναν λιγότερο φιλόδοξο στόχο: την παρασκευή εμβολίων.
Όταν χτύπησε η COVID-19, η Moderna ενήργησε γρήγορα, δημιουργώντας από τον ιό ένα πρωτότυπο εμβόλιο μέσα σε λίγες ημέρες. Η αλληλουχία γονιδιώματος είναι διαθέσιμη στο διαδίκτυο. Στη συνέχεια, η εταιρεία συνεργάστηκε με το Εθνικό Ινστιτούτο Αλλεργιών και Λοιμωδών Νοσημάτων των ΗΠΑ (NIAID) για τη διεξαγωγή μελετών σε ποντίκια και την έναρξη δοκιμών σε ανθρώπους: όλα αυτά σε λιγότερο από δέκα εβδομάδες. Η BioNTech ακολούθησε παρόμοια προσέγγιση και τον Μάρτιο του 2020 συνεργάστηκε με τη φαρμακευτική εταιρεία Pfizer που έχει έδρα στη Νέα Υόρκη: οι κλινικές δοκιμές προχώρησαν με ρυθμό ρεκόρ, περνώντας από την πρώτη δοκιμή στον άνθρωπο στην έγκριση έκτακτης ανάγκης σε λιγότερο από οκτώ μήνες. Και τα δύο εγκεκριμένα εμβόλια χρησιμοποιούν τροποποιημένο mRNA διαμορφωμένο σε LNP. Και τα δύο περιέχουν επίσης αλληλουχίες που κωδικοποιούν μια μορφή της πρωτεΐνης αιχμής SARS-CoV-2 η οποία υιοθετεί ένα σχήμα πιο επιδεκτικό για την πρόκληση προστατευτικής ανοσίας. Πολλοί ειδικοί λένε ότι η τροποποίηση της πρωτεΐνης, που επινοήθηκε από τον εμβολιολόγο Barney Graham, τους δομικούς βιολόγους Jason McLellan στο Πανεπιστήμιο του Τέξας στο Όστιν και τον Andrew Ward στην ερευνητική εταιρεία Scripps, είναι επίσης μια συνεισφορά που αξίζει να σημειωθεί.
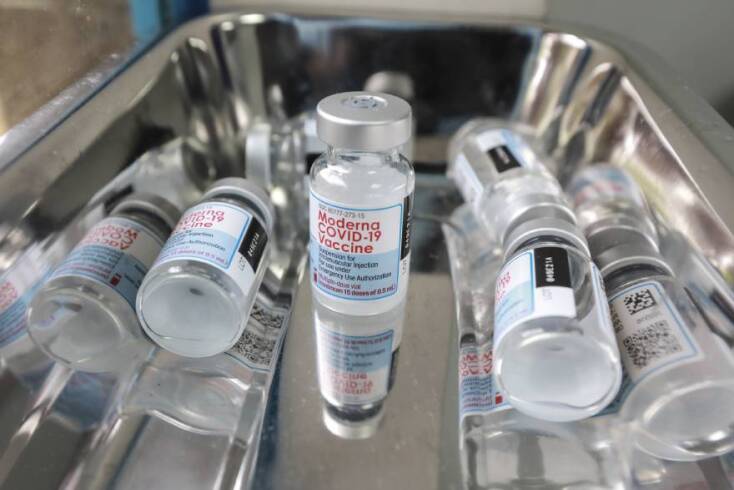
Η Moderna, ο κυρίαρχος παίκτης στον τομέα του εμβολίου mRNA, διενεργεί τώρα πειραματικές κλινικές δοκιμές για την αντιμετώπιση της γρίπης και μιας σειράς άλλων μολυσματικών ασθενειών. Με λίγα λόγια, ο COVID ξεκλείδωσε τη δύναμη των εμβολίων RNA και το μέλλον φαίνεται πάρα πολύ αισιόδοξο. Όσο για τη συζήτηση για το Νόμπελ, το σύγχρονο τοπίο της παγκοσμιοποιημένης επιστήμης καθιστά αρκετά δύσκολη τη βράβευση ενός ανθρώπου ή ενός εργαστηρίου -εξάλλου, αυτό που έχει σπουδαιότητα για τους ανθρώπους δεν είναι ποιος θα βραβευτεί αλλά το πώς το mRNA μπορεί να τους απαλλάξει από μια σειρά παθογόνα, επιδημίες και πανδημίες.
ΤΑ ΠΙΟ ΔΗΜΟΦΙΛΗ

ΔΙΑΒΑΖΟΝΤΑΙ ΠΑΝΤΑ
ΔΕΙΤΕ ΕΠΙΣΗΣ
Τι πρέπει να αλλάξετε την επόμενη φορά που θα γυρίσετε από το σούπερ μάρκετ
Η σύνδεση με τις ημικρανίες, ποιοι είναι πιο επιρρεπείς
Δεν οφείλεται μόνο στη στάση ύπνου - Συνδέεται άμεσα με την ικανότητα του ανθρώπου να μιλά
Ποιους αφορά, πότε θα είναι διαθέσιμo
Το 38% του ενήλικου πληθυσμού είναι χρήστες καπνικών προϊόντων
Οι επιστήμονες χρησιμοποιούν τον όρο «υψηλός πνευμονογαστρικός τόνος»
Η σημασία της διατροφής και της άσκησης
Νάρθηκες, φυσικοθεραπεία και η επιλογή της επέμβασης
Πώς η απλή καταγραφή των σκέψεων και των συναισθημάτων μας θωρακίζει απέναντι στο στρες
Η περίπτωση ενός άντρα που υπέστη σπάνια αλλεργική αντίδραση
Όταν η κούραση είναι κάτι περισσότερο από ανθρώπινη κατάσταση
Φυσικά η τεχνολογία δεν μπορεί να αντικαταστήσει την ανθρώπινη φροντίδα
Έρευνες δείχνουν ότι περίπου 1 στους 4 δεν εμφανίζει καθόλου συμπτώματα, ακόμη και μετά από βαριά κατανάλωση αλκοόλ
Η επαφή με το περιβάλλον μειώνει άμεσα το στρες, ρυθμίζει ορμόνες, ενισχύει το ανοσοποιητικό και βελτιώνει τη διάθεση
Οι τεχνικές που ηρεμούν το σώμα και τον νου όταν οι αρνητικές σκέψεις κυριαρχούν στην καθημερινότητα
Η κλινική δοκιμή περιέλαβε περισσότερους από 4.400 ασθενείς
Η δημοφιλής μέθοδος δροσιάς που τελικά χαλάει τον ύπνο - Πώς να τον χρησιμοποιήσετε σωστά
Eιδικοί εξηγούν γιατί το βάδισμα είναι το θεμέλιο της ευεξίας και πώς προστατεύει σώμα και πνεύμα
Επιστήμονες ανακάλυψαν ότι τα έντομα συνδέουν τη μυρωδιά του DEET με την τροφή, ανατρέποντας όσα ξέραμε
Με επίκεντρο το μέλλον της ογκολογικής φροντίδας
Έχετε δει 20 από 200 άρθρα.